Химия 8 Класс Свойства Оксидов softruwholesale
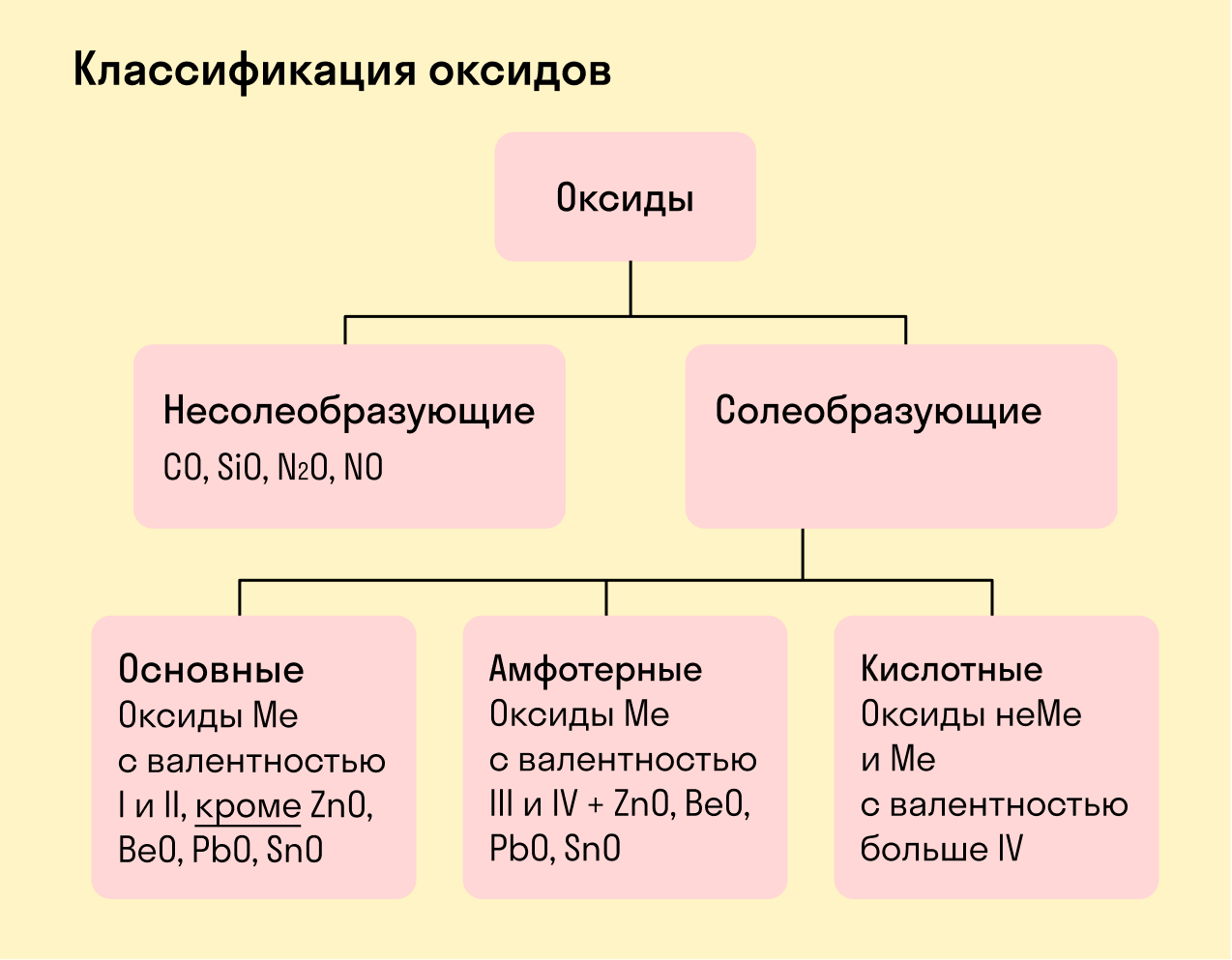
Несолеобразующие оксиды что это значит
Соединения, которые содержат атомы кислорода, соединённые между собой, называют пероксидами или перекисями (содержат цепочку −O−O−), супероксидами (или надпероксидами, содержат группу О −. 2) и озонидами (содержат группу О −. 3 ). Они, строго говоря, не относятся к категории оксидов.

Тема №10 «Характерные химические свойства основных, амфотерных и кислотных оксидов»
Определение оксидов. Оксиды — это сложные вещества, состоящие из двух химических элементов (т. е. бинарные соединения), один из которых — кислород в степени окисления −2. Общая.

Кислотные оксиды Ektpol
Химические свойства оксидов; Свойства галогенов; Обменные реакции; Химические свойства средних и кислых солей; Свойства нерастворимых соединений; Свойства аммиака
Оксиды. Классификация, химические и физические свойства. Определение групп оксидов. Получение
Какие вещества называются оксидами? Как вы думаете, какова тема сегодняшнего урока? 2. Изучение новой темы. А) Классификация оксидов. ТАБЛИЦА. Б) Химические свойства оксидов. ТАБЛИЦА. 3.Физкультминутка.

Химические свойства оксидов презентация онлайн
Химические свойства основных оксидов. Основными оксидами называются оксиды, которым соответствуют основания. Например, основным оксидам k 2 o, Сao соответствуют основания koh, ca(oh) 2. Рис. 2.

Химические свойства кислот солей оксидов и оснований Свойства оксидов, кислот, оснований и
Химические свойства оксидов; Свойства галогенов; Обменные реакции; Химические свойства средних и кислых солей; Свойства нерастворимых соединений; Свойства аммиака

46. Неорганическая химия. Тема 6. Неорганические соединения. Часть 5. Свойства амфотерных
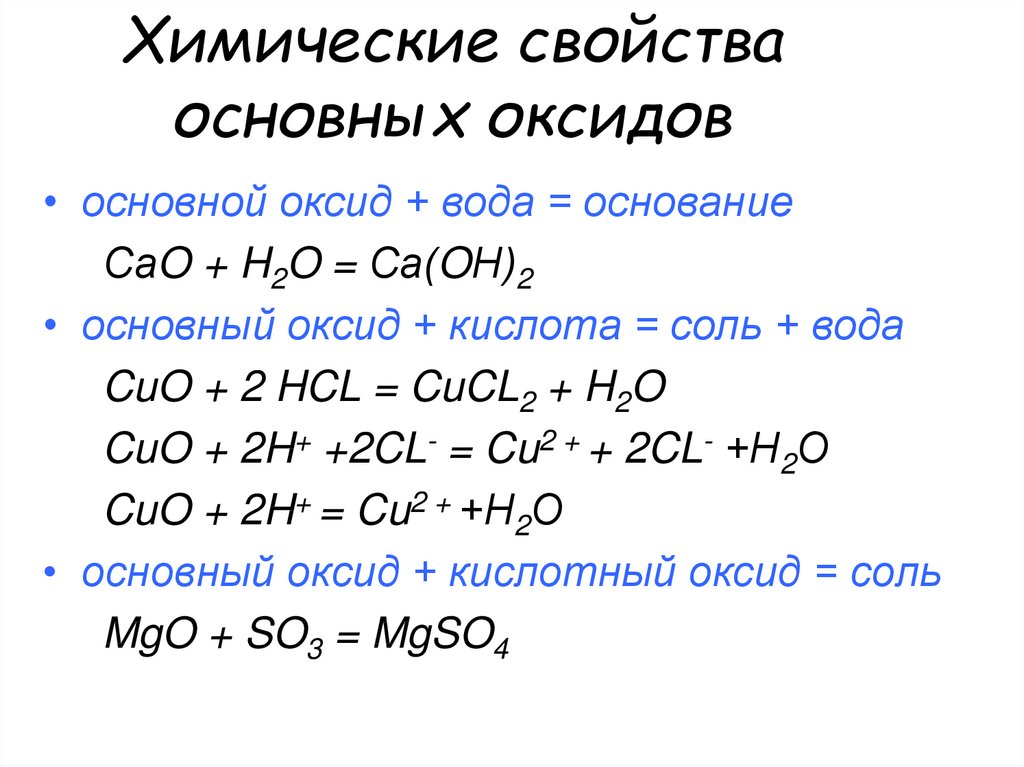
Химические свойства оксидов. Теория: 1. Основные оксиды, образованные щелочными и щелочноземельными металлами, взаимодействуют с водой, образуя растворимое в воде основание — щёлочи. Основный оксид + вода → основание. Например, при взаимодействии оксида кальция с водой образуется гидроксид кальция: CaO +H2O → Ca(OH)2. 2.
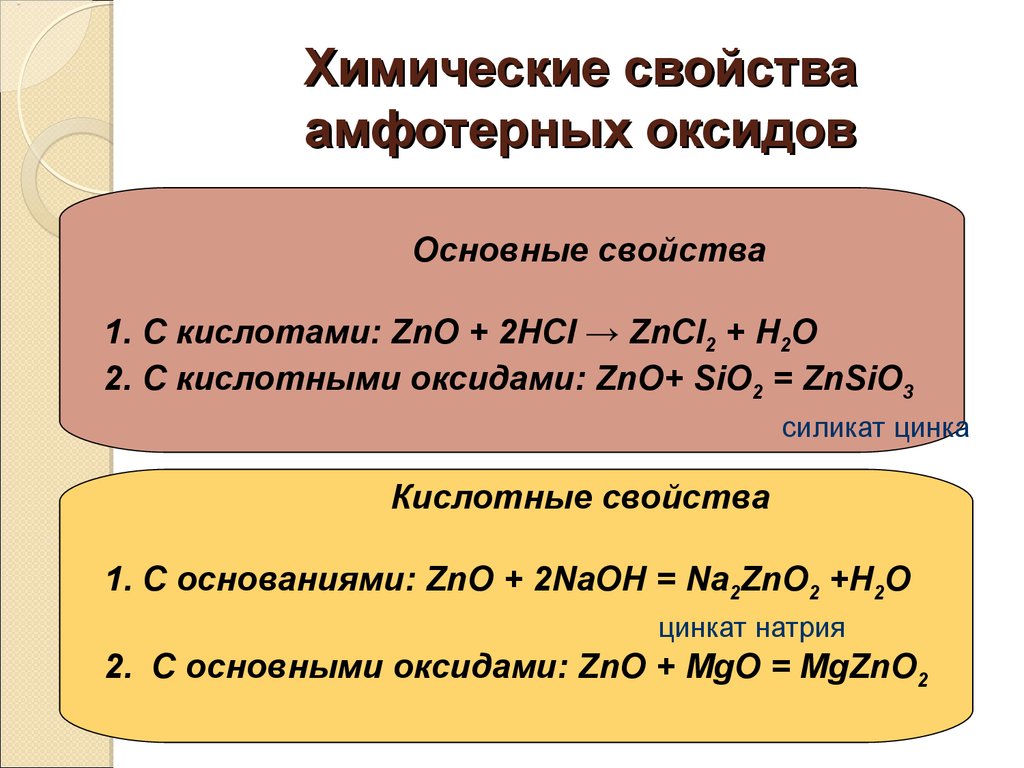
Классы неорганических веществ презентация онлайн
Классификация оксидов. Химические свойства оксидов. Примеры реакции. Основные оксиды. 1. Основной оксид* + вода —> щелочь. К 2 О + Н 2 О → 2КОН, ВаО + Н 2 o → Ва(ОН) 2. 2. Основной оксид + кислота.

Химия 8 Класс Свойства Оксидов softruwholesale
Химические свойства основных оксидов. Подробно про химические свойства оксидов можно прочитать в соответствующих статьях: Химические свойства основных оксидов.

Химические свойства спиртов (таблица) Химия онлайн
Основные оксиды — (Оксиды металлов — na 2 o, cao, cuo и т д) Кислотные оксиды — (Оксиды неметаллов, а так же оксиды металлов в степени окисления v-vii — mn 2 o 7,co 2, n 2 o 5, so 2, so 3 и т д)
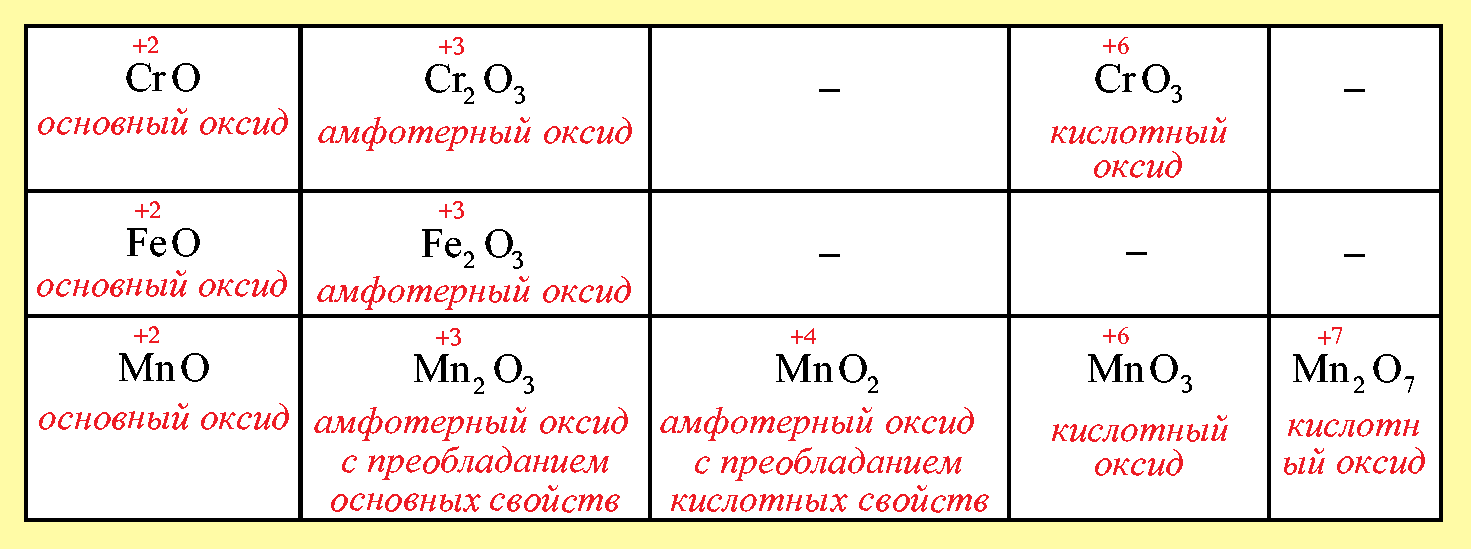
Таблица физические свойства оксидов применение
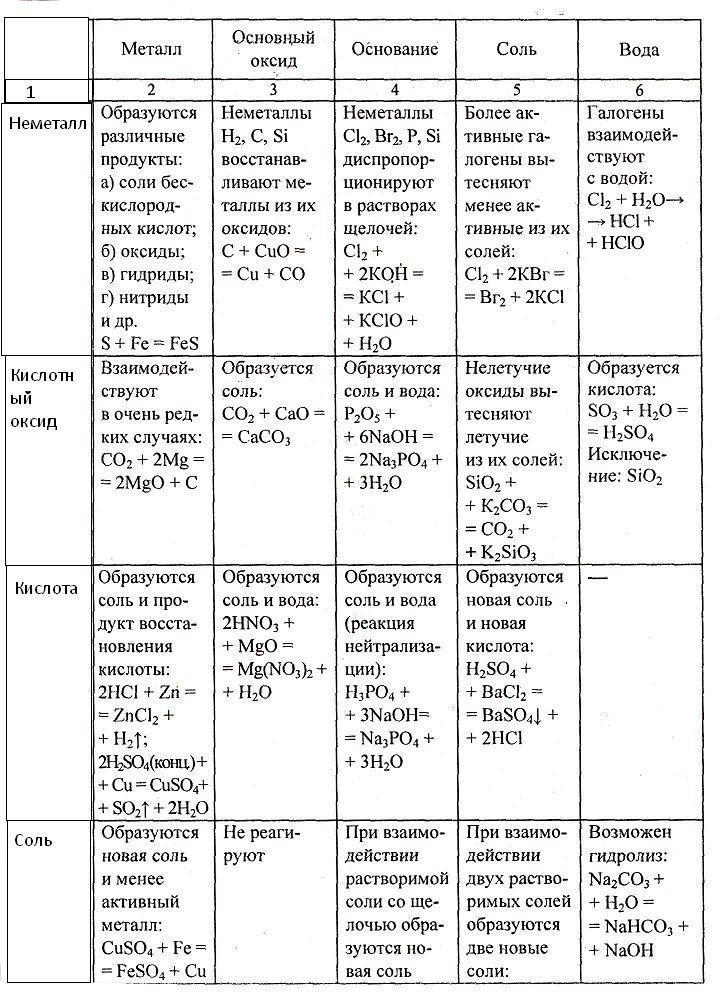
Схема классификация оксидов; Таблица классификация оксидов с примерами; Способы получения оксидов таблица; Химические свойства оксидов таблица

Опорный конспект по химии; Свойства оксидов; УчительPRO
Таблица химических формул; Химические свойства основных оксидов; Химические свойства кислотных оксидов

Подготовка к ЕГЭ по химии 2021 6(Б) Химические свойства оксидов
К активным основным оксидам отнесем оксиды щелочных и щелочноземельных металлов (все элементы IA и IIA групп, кроме водорода H, бериллия Be и магния Mg). Например, Na 2 O, CaO, Rb 2 O, SrO и т.д. К малоактивным основным оксидам отнесем все основные оксиды, которые не попали в список активных основных оксидов. Например, FeO, CuO, CrO и т.д.
С какими из перечисленных веществ будет реагировать азотная кислота H2O Ca(OH)2 K2O H2SO4 O2
Оксиды — сложные вещества, молекулы которых состоят из атомов двух химических элементов, один из которых — кислород. Атом кислорода в оксидах всегда имеет степень окисления -2. К примеру, оксидом является соединение P2O5.
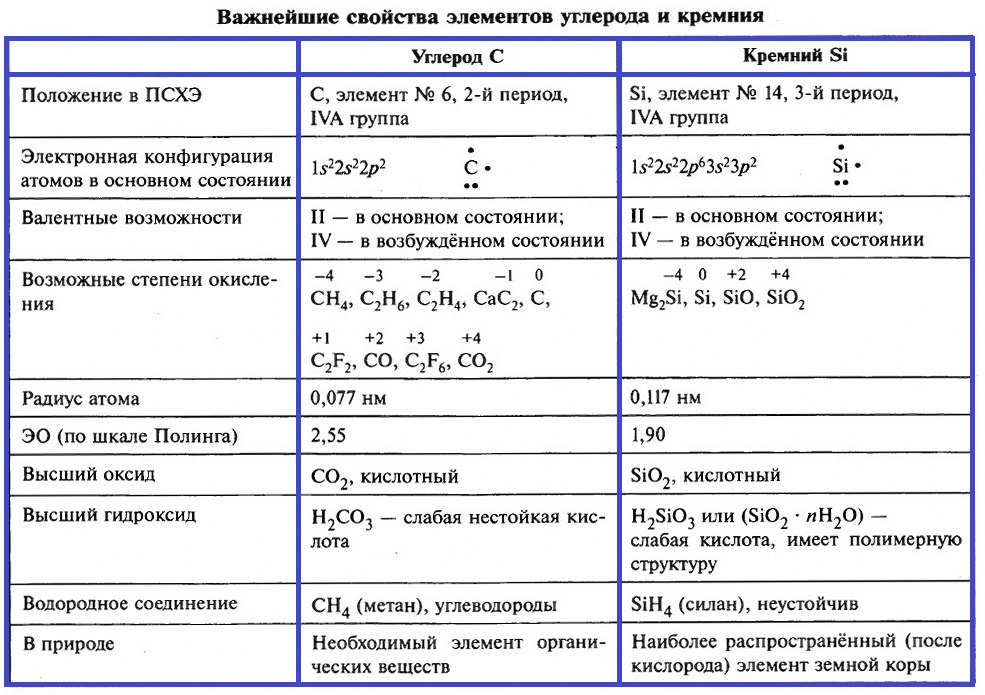
Углерод и кремний. Элементы IVAгруппы. Конспект УчительPRO
все реакции для ОГЭ и ЕГЭ по химии, тренажеры составления химических реакций, правила окислительно-восстановительных реакций

Оксиды их классификация способы получения и химические свойства таблица схема
В зависимости от химических свойств различают: — солеобразующие оксиды: основные оксиды. К ним относятся оксиды металлов, степень окисления которых +1, + 2; кислотные оксиды. К ним относятся оксиды металлов со степенью окисления +5, + 6, + 7, и оксиды неметаллов; амфотерные оксиды.